Structura atomului de iod (I), schemă și exemple
Informații generale despre structura atomului de iod
Se referă la elemente ale familiei p. Metaloid. Denumire - I. Număr ordinal - 53. Masă atomică relativă - 126.905 a.m.u.
Structura electronică a atomului de iod
Atomul de iod este format dintr-un nucleu încărcat pozitiv (+53), în interiorul căruia se află 53 de protoni și 74 de neutroni, iar 53 de electroni se mișcă pe cinci orbite.
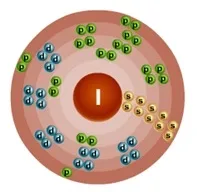
Fig.1. Structura schematică a atomului de iod.
Distribuția electronilor în orbitali este următoarea:
Nivelul de energie exterior al atomului de iod conține 7 electroni, care sunt valență. Diagrama energetică a stării fundamentale ia următoarea formă:
Electronii de valență ai unui atom de iod pot fi caracterizați printr-un set de patru numere cuantice: n (cuanta principală), l (orbital), ml (magnetic) și s (spin):
Exemple de rezolvare a problemelor
| Exercițiu | Configurația electronică 1s 2 2s 2 2p 6 corespunde unui atom de fluor, unui atom de sodiu, unui ion oxid sau unui ion sulfură? |
| Soluţie | Să notăm formulele electronice ale atomilor și ionilor propuși ca răspunsuri: |
Pe baza acestui lucru, concluzionăm că sarcina indică configurația electronică a ionului de oxid.
| Exercițiu | Configurația electronică 1s 2 2s 2 corespunde particulei: C 4-, C 4+, C 2+ sau C 2-. |
| Soluţie | Un atom de carbon în starea sa fundamentală are 6 electroni. Configurația sa electronică va arăta astfel: |
În formarea cationilor, elementul acționează ca un donor de protoni, adică. numărul total de electroni scade; cantitatecrește. În comparație cu starea fundamentală, numărul total de electroni din învelișul de electroni a scăzut cu 2. Prin urmare, aceasta este o particulă C 2+.